Le monde dans lequel nous vivons est d'une beauté inimaginable et plein de nombreux processus différents qui définissent le cours de la vie. Tous ces processus sont étudiés par la science familière - la physique. C'est l'occasion de se faire au moins une idée de l'origine de l'univers. Dans cet article, nous examinerons un concept tel que la théorie cinétique moléculaire, ses équations, types et formules. Cependant, avant de passer à une étude plus approfondie de ces questions, vous devez clarifier par vous-même le sens même de la physique et les domaines qu'elle étudie.
Qu'est-ce que la physique ?

En fait, il s'agit d'une science très vaste et, peut-être, l'une des plus fondamentales de l'histoire de l'humanité. Par exemple, si la même science informatique est associée à presque tous les domaines de l'activité humaine, qu'il s'agisse de conception informatique ou de création de dessins animés, alors la physique est la vie elle-même, une description de ses processus et flux complexes. Essayons de comprendre sa signification, en simplifiant au maximum la compréhension.
AlorsAinsi, la physique est une science qui traite de l'étude de l'énergie et de la matière, des liens entre elles, de l'explication de nombreux processus se produisant dans notre vaste univers. La théorie moléculaire-cinétique de la structure de la matière n'est qu'une petite goutte dans la mer des théories et des branches de la physique.
L'énergie, que cette science étudie en détail, peut être représentée sous diverses formes. Par exemple, sous forme de lumière, de mouvement, de gravité, de rayonnement, d'électricité et de nombreuses autres formes. Nous aborderons dans cet article la théorie cinétique moléculaire de la structure de ces formes.
L'étude de la matière nous donne une idée de la structure atomique de la matière. Soit dit en passant, cela découle de la théorie moléculaire-cinétique. La science de la structure de la matière nous permet de comprendre et de trouver le sens de notre existence, les raisons de l'émergence de la vie et de l'Univers lui-même. Essayons encore d'étudier la théorie de la cinétique moléculaire de la matière.
Tout d'abord, une introduction est nécessaire pour bien comprendre la terminologie et toute conclusion.
Sujets de physique
Pour répondre à la question de savoir ce qu'est la théorie de la cinétique moléculaire, on ne peut que parler de sections de la physique. Chacun d'eux traite de l'étude détaillée et de l'explication d'un domaine particulier de la vie humaine. Ils sont classés comme suit:
- Mécanique, qui est divisée en deux autres sections: cinématique et dynamique.
- Statique.
- Thermodynamique.
- Section moléculaire.
- Électrodynamique.
- Optique.
- Physique des quantums et du noyau atomique.
Parlons spécifiquement de moléculairephysique, car elle est basée sur la théorie moléculaire-cinétique.
Qu'est-ce que la thermodynamique ?
En général, la partie moléculaire et la thermodynamique sont des branches étroitement liées de la physique, qui étudient exclusivement la composante macroscopique du nombre total de systèmes physiques. Il convient de rappeler que ces sciences décrivent précisément l'état interne des corps et des substances. Par exemple, leur état lors du chauffage, de la cristallisation, de la vaporisation et de la condensation, au niveau atomique. En d'autres termes, la physique moléculaire est la science des systèmes constitués d'un grand nombre de particules: atomes et molécules.
Ce sont ces sciences qui ont étudié les principales dispositions de la théorie de la cinétique moléculaire.
Même au cours de la septième année, nous nous sommes familiarisés avec les concepts de micro- et macro-mondes, de systèmes. Il ne sera pas superflu de rafraîchir ces termes en mémoire.
Le micromonde, comme on peut le voir d'après son nom même, est composé de particules élémentaires. En d'autres termes, c'est le monde des petites particules. Leurs tailles sont mesurées dans la plage de 10-18 m à 10-4 m, et le temps de leur état réel peut atteindre à la fois l'infini et intervalles disproportionnellement petits, par exemple, 10-20 s.
Macroworld considère des corps et des systèmes de formes stables, constitués de nombreuses particules élémentaires. De tels systèmes sont à la mesure de notre taille humaine.
De plus, il existe un méga monde. Il est composé d'énormes planètes, de galaxies cosmiques et de complexes.
Basesthéorie
Maintenant que nous avons récapitulé un peu et rappelé les termes de base de la physique, nous pouvons passer directement au sujet principal de cet article.
La théorie moléculaire-cinétique est apparue et a été formulée pour la première fois au XIXe siècle. Son essence réside dans le fait qu'il décrit en détail la structure de toute substance (plus souvent la structure des gaz que des corps solides et liquides), sur la base de trois dispositions fondamentales qui ont été recueillies à partir des hypothèses d'éminents scientifiques tels que Robert Hooke, Isaac Newton, Daniel Bernoulli, Mikhail Lomonossov et bien d'autres.
Les principales dispositions de la théorie de la cinétique moléculaire ressemblent à ceci:
- Absolument toutes les substances (qu'elles soient liquides, solides ou gazeuses) ont une structure complexe, constituée de particules plus petites: molécules et atomes. Les atomes sont parfois appelés "molécules élémentaires".
- Toutes ces particules élémentaires sont toujours dans un état de mouvement continu et chaotique. Chacun de nous a rencontré une preuve directe de cette proposition, mais, très probablement, n'y a pas attaché beaucoup d'importance. Par exemple, nous avons tous vu dans le contexte des rayons du soleil que les particules de poussière se déplacent constamment dans une direction chaotique. Cela est dû au fait que les atomes produisent des poussées mutuelles les uns avec les autres, se transmettant constamment de l'énergie cinétique. Ce phénomène a été étudié pour la première fois en 1827, et il a été nommé d'après le découvreur - "mouvement brownien".
- Toutes les particules élémentaires sont en processus d'interaction continue les unes avec les autres aveccertaines forces qui ont un rock électrique.
Il convient de noter qu'un autre exemple décrivant la position numéro deux, qui peut également s'appliquer, par exemple, à la théorie de la cinétique moléculaire des gaz, est la diffusion. Nous le rencontrons dans la vie de tous les jours, et dans de multiples tests et contrôles, il est donc important d'en avoir une idée.
Premièrement, considérez les exemples suivants:
Le médecin a accidentellement renversé de l'alcool d'un flacon sur la table. Ou peut-être avez-vous laissé tomber votre flacon de parfum et il s'est répandu sur le sol.
Pourquoi, dans ces deux cas, à la fois l'odeur d'alcool et l'odeur de parfum rempliront toute la pièce après un certain temps, et pas seulement la zone où le contenu de ces substances a été renversé ?
La réponse est simple: diffusion.
Diffusion - qu'est-ce que c'est ? Comment ça se passe ?

Il s'agit d'un processus dans lequel les particules qui composent une substance particulière (généralement un gaz) pénètrent dans les vides intermoléculaires d'une autre. Dans nos exemples ci-dessus, il s'est passé ce qui suit: en raison d'un mouvement thermique, c'est-à-dire continu et dissocié, des molécules d'alcool et/ou de parfum sont tombées dans les interstices entre les molécules d'air. Peu à peu, sous l'influence de la collision avec des atomes et des molécules d'air, ils se sont répandus dans la pièce. Soit dit en passant, l'intensité de la diffusion, c'est-à-dire la vitesse de son écoulement, dépend de la densité des substances impliquées dans la diffusion, ainsi que de l'énergie de mouvement de leurs atomes et molécules, appelée cinétique. Plus l'énergie cinétique est élevée, plus la vitesse de ces molécules, respectivement, et l'intensité sont élevées.
Le processus de diffusion le plus rapide peut être appelé diffusion dans les gaz. Cela est dû au fait que le gaz n'est pas homogène dans sa composition, ce qui signifie que les vides intermoléculaires dans les gaz occupent respectivement une quantité importante d'espace et que le processus d'introduction d'atomes et de molécules d'une substance étrangère se déroule plus facilement et plus rapidement..
Ce processus est un peu plus lent dans les liquides. La dissolution de morceaux de sucre dans une tasse de thé n'est qu'un exemple de la diffusion d'un solide dans un liquide.
Mais le temps le plus long est celui de la diffusion dans les corps à structure cristalline solide. C'est exactement le cas, car la structure des solides est homogène et possède un réseau cristallin fort, dans les cellules duquel les atomes du solide vibrent. Par exemple, si les surfaces de deux barres métalliques sont bien nettoyées puis mises en contact l'une avec l'autre, alors après un temps suffisamment long nous pourrons détecter des morceaux d'un métal dans l'autre, et vice versa.
Comme toute autre section fondamentale, la théorie fondamentale de la physique est divisée en parties distinctes: classification, types, formules, équations, etc. Ainsi, nous avons appris les bases de la théorie de la cinétique moléculaire. Cela signifie que vous pouvez procéder en toute sécurité à l'examen de blocs théoriques individuels.
Théorie moléculaire-cinétique des gaz
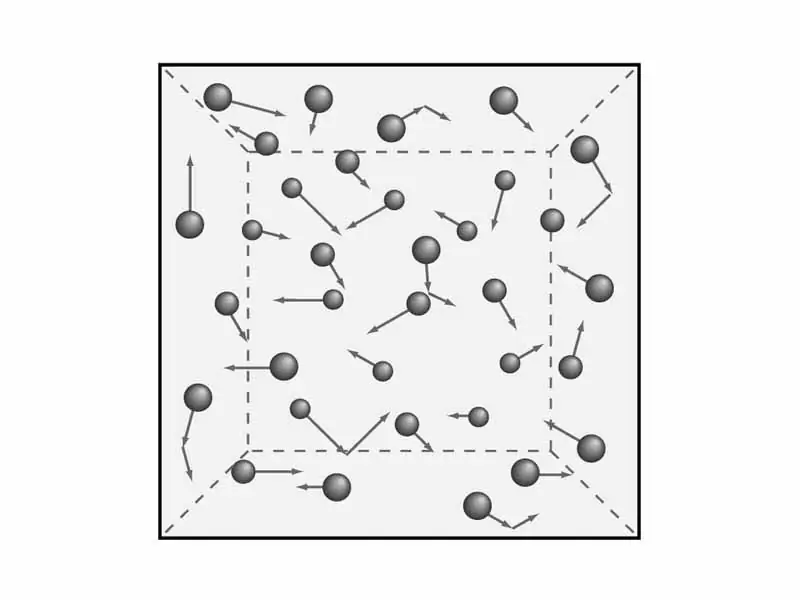
Il est nécessaire de comprendre les dispositions de la théorie des gaz. Comme nous l'avons dit précédemment, nous considérerons les caractéristiques macroscopiques des gaz, telles que la pression et la température. C'estseront nécessaires plus tard pour dériver l'équation de la théorie cinétique moléculaire des gaz. Mais les mathématiques - plus tard, et maintenant abordons la théorie et, par conséquent, la physique.
Les scientifiques ont formulé cinq dispositions de la théorie moléculaire des gaz, qui servent à comprendre le modèle cinétique des gaz. Ils sonnent comme ceci:
- Tous les gaz sont constitués de particules élémentaires qui n'ont pas une certaine taille, mais une certaine masse. En d'autres termes, le volume de ces particules est minime par rapport à la longueur qui les sépare.
- Les atomes et les molécules de gaz n'ont pratiquement pas d'énergie potentielle, respectivement, selon la loi, toute énergie est égale à cinétique.
- Nous nous sommes déjà familiarisés avec cette position plus tôt - mouvement brownien. Autrement dit, les particules de gaz sont toujours en mouvement continu et chaotique.
- Absolument toutes les collisions mutuelles de particules de gaz, accompagnées du message de vitesse et d'énergie, sont complètement élastiques. Cela signifie qu'il n'y a pas de perte d'énergie ou de sauts brusques de leur énergie cinétique lors d'une collision.
- Dans des conditions normales et à température constante, l'énergie moyenne du mouvement des particules de presque tous les gaz est la même.
On peut réécrire la cinquième position à travers ce type d'équation de la théorie moléculaire-cinétique des gaz:
E=1/2mv^2=3/2kT, où k est la constante de Boltzmann; T - température en Kelvin.
Cette équation nous fait comprendre la relation entre la vitesse des particules élémentaires de gaz et leur température absolue. En conséquence, plus leur valeur absolue est élevéetempérature, plus leur vitesse et leur énergie cinétique sont élevées.
Pression de gaz
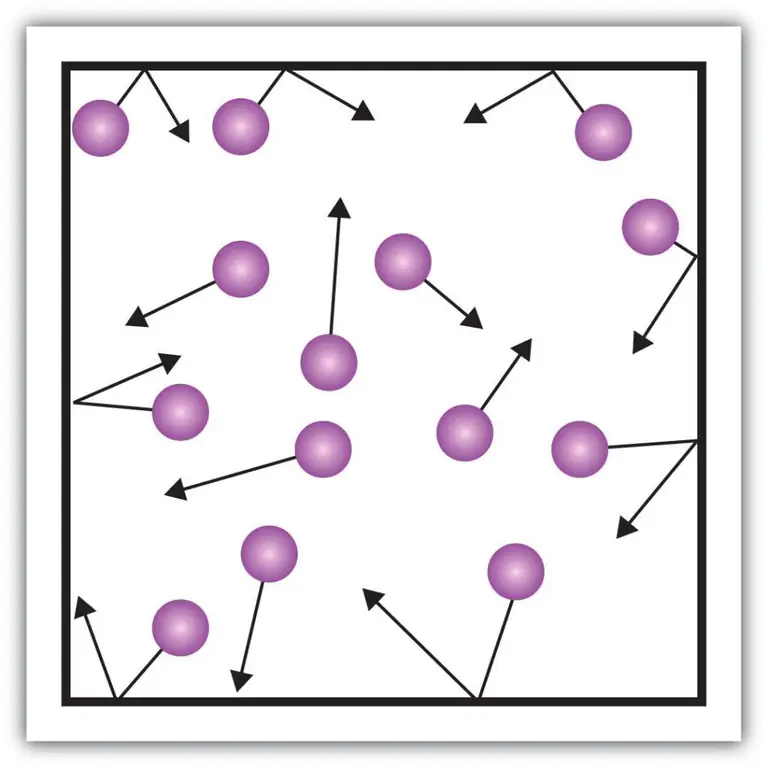
De telles composantes macroscopiques de la caractéristique, telles que la pression des gaz, peuvent également être expliquées à l'aide de la théorie cinétique. Pour ce faire, imaginons l'exemple suivant.
Supposons qu'une molécule d'un gaz se trouve dans une boîte dont la longueur est L. Utilisons les dispositions de la théorie des gaz décrites ci-dessus et tenons compte du fait que la sphère moléculaire ne se déplace que le long de x -axe. Ainsi, nous pourrons observer le processus de collision élastique avec l'une des parois du vaisseau (boîte).
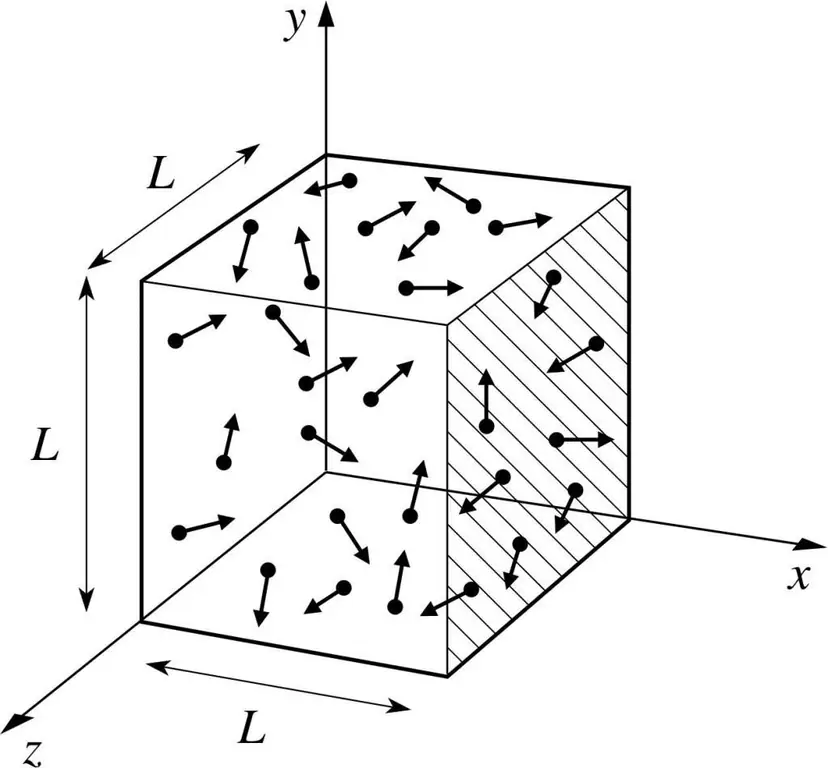
L'impulsion de la collision en cours, comme nous le savons, est déterminée par la formule: p=mv, mais dans ce cas, cette formule prendra une forme de projection: p=mv(x).
Puisque nous ne considérons que la dimension de l'axe des x, c'est-à-dire l'axe des x, la variation totale de la quantité de mouvement sera exprimée par la formule: mv(x) - m(-v(x))=2mv(x).
Ensuite, considérons la force exercée par notre objet en utilisant la deuxième loi de Newton: F=ma=P/t.
À partir de ces formules, nous exprimons la pression côté gaz: P=F/a;
Maintenant, substituons l'expression de la force dans la formule résultante et obtenons: P=mv(x)^2/L^3.
Après cela, notre formule de pression finie peut être écrite pour le N-ème nombre de molécules de gaz. En d'autres termes, cela ressemblera à ceci:
P=Nmv(x)^2/V, où v est la vitesse et V le volume.
Essayons maintenant de souligner quelques dispositions de base sur la pression du gaz:
- Il se manifeste à traverscollisions de molécules avec des molécules des parois de l'objet dans lequel il se trouve.
- L'amplitude de la pression est directement proportionnelle à la force et à la vitesse d'impact des molécules sur les parois du vaisseau.
Quelques brèves conclusions sur la théorie
Avant d'aller plus loin et d'examiner l'équation de base de la théorie de la cinétique moléculaire, nous vous proposons quelques brèves conclusions à partir des points et de la théorie ci-dessus:
- La mesure de l'énergie moyenne de mouvement de ses atomes et molécules est la température absolue.
- Lorsque deux gaz différents sont à la même température, leurs molécules ont la même énergie cinétique moyenne.
- L'énergie des particules de gaz est directement proportionnelle à la vitesse quadratique moyenne: E=1/2mv^2.
- Bien que les molécules de gaz aient respectivement une énergie cinétique moyenne et une vitesse moyenne, les particules individuelles se déplacent à des vitesses différentes: certaines rapides, d'autres lentes.
- Plus la température est élevée, plus la vitesse des molécules est élevée.
- Combien de fois nous augmentons la température du gaz (par exemple, double), l'énergie de mouvement de ses particules augmente autant de fois (respectivement, double).
Équation et formules de base

L'équation de base de la théorie de la cinétique moléculaire vous permet d'établir la relation entre les quantités du micromonde et, par conséquent, les quantités macroscopiques, c'est-à-dire mesurées.
L'un des modèles les plus simples que la théorie moléculaire puisse considérer est le modèle des gaz parfaits.
On pourrait dire quec'est une sorte de modèle imaginaire étudié par la théorie de la cinétique moléculaire d'un gaz parfait, dans lequel:
- les particules de gaz les plus simples sont considérées comme des boules parfaitement élastiques qui interagissent à la fois entre elles et avec les molécules des parois de n'importe quel récipient dans un seul cas - une collision absolument élastique;
- les forces d'attraction à l'intérieur du gaz sont absentes, ou elles peuvent en fait être négligées;
- les éléments de la structure interne du gaz peuvent être considérés comme des points matériels, c'est-à-dire que leur volume peut également être négligé.
Considérant un tel modèle, le physicien d'origine allemande Rudolf Clausius a écrit une formule pour la pression du gaz à travers la relation entre les paramètres microscopiques et macroscopiques. Il ressemble à:
p=1/3m(0)nv^2.
Plus tard, cette formule sera appelée l'équation de base de la théorie moléculaire-cinétique d'un gaz parfait. Il peut se présenter sous plusieurs formes différentes. Notre devoir est maintenant de montrer des sections telles que la physique moléculaire, la théorie de la cinétique moléculaire, et donc leurs équations et types complets. Par conséquent, il est logique d'envisager d'autres variantes de la formule de base.
On sait que l'énergie moyenne caractérisant le mouvement des molécules de gaz peut être trouvée à l'aide de la formule: E=m(0)v^2/2.
Dans ce cas, nous pouvons remplacer l'expression m(0)v^2 dans la formule de pression d'origine par l'énergie cinétique moyenne. De ce fait, nous aurons l'opportunité de composer l'équation de base de la théorie de la cinétique moléculaire des gaz sous la forme suivante: p=2/3nE.
D'ailleurs, nous savons tous que l'expression m(0)n peut s'écrire comme un produit de deux quotients:
m/NN/V=m/V=ρ.
Après ces manipulations, nous pouvons réécrire notre formule pour l'équation de la théorie cinétique moléculaire d'un gaz parfait sous une troisième forme différente:
p=1/3ρv^2.
Eh bien, c'est peut-être tout ce que vous devez savoir sur ce sujet. Il ne reste plus qu'à systématiser les connaissances acquises sous forme de brèves (et pas si) conclusions.
Toutes les conclusions générales et les formules sur le thème "Théorie moléculaire-cinétique"
Alors commençons.
Premier:
La physique est une science fondamentale incluse dans le cours des sciences naturelles, qui étudie les propriétés de la matière et de l'énergie, leur structure, les schémas de la nature inorganique.
Il comprend les sections suivantes:
- mécanique (cinématique et dynamique);
- statique;
- thermodynamique;
- électrodynamique;
- section moléculaire;
- optique;
- physique des quantums et du noyau atomique.
Deuxième:
La physique des particules et la thermodynamique sont des branches étroitement liées qui étudient la composante exclusivement macroscopique du nombre total de systèmes physiques, c'est-à-dire les systèmes constitués d'un grand nombre de particules élémentaires.
Ils sont basés sur la théorie de la cinétique moléculaire.
Troisième:
Le nœud du problème est le suivant. La théorie de la cinétique moléculaire décrit en détail la structure d'une substance (plus souvent la structure des gaz que celle des solides).et corps liquides), sur la base de trois hypothèses fondamentales qui ont été recueillies à partir des hypothèses d'éminents scientifiques. Parmi eux: Robert Hooke, Isaac Newton, Daniel Bernoulli, Mikhail Lomonosov et bien d'autres.
Quatrième:
Trois principes de base de la théorie de la cinétique moléculaire:
- Toutes les substances (qu'elles soient liquides, solides ou gazeuses) ont une structure complexe composée de particules plus petites: molécules et atomes.
- Toutes ces particules simples sont en mouvement chaotique continu. Exemple: mouvement brownien et diffusion.
- Toutes les molécules dans toutes les conditions interagissent les unes avec les autres avec certaines forces qui ont une roche électrique.
Chacune de ces dispositions de la théorie de la cinétique moléculaire est une base solide dans l'étude de la structure de la matière.
Cinquième:
Plusieurs points principaux de la théorie moléculaire pour le modèle de gaz:
- Tous les gaz sont constitués de particules élémentaires qui n'ont pas une certaine taille, mais une certaine masse. En d'autres termes, le volume de ces particules est minime par rapport aux distances qui les séparent.
- Les atomes et les molécules de gaz n'ont pratiquement pas d'énergie potentielle, respectivement, leur énergie totale est égale à l'énergie cinétique.
- Nous nous sommes déjà familiarisés avec cette position plus tôt - mouvement brownien. Autrement dit, les particules de gaz sont toujours en mouvement continu et aléatoire.
- Absolument toutes les collisions mutuelles d'atomes et de molécules de gaz, accompagnées du message de vitesse et d'énergie, sont complètement élastiques. C'estsignifie qu'il n'y a pas de perte d'énergie ou de sauts brusques de leur énergie cinétique lors d'une collision.
- Dans des conditions normales et à température constante, l'énergie cinétique moyenne de presque tous les gaz est la même.
Sixième:
Conclusions de la théorie sur les gaz:
- La température absolue est une mesure de l'énergie cinétique moyenne de ses atomes et molécules.
- Lorsque deux gaz différents sont à la même température, leurs molécules ont la même énergie cinétique moyenne.
- L'énergie cinétique moyenne des particules de gaz est directement proportionnelle à la vitesse quadratique moyenne: E=1/2mv^2.
- Bien que les molécules de gaz aient respectivement une énergie cinétique moyenne et une vitesse moyenne, les particules individuelles se déplacent à des vitesses différentes: certaines rapides, d'autres lentes.
- Plus la température est élevée, plus la vitesse des molécules est élevée.
- Combien de fois nous augmentons la température du gaz (par exemple, double), l'énergie cinétique moyenne de ses particules augmente également autant de fois (respectivement, double).
- La relation entre la pression d'un gaz sur les parois du récipient dans lequel il se trouve et l'intensité des impacts des molécules sur ces parois est directement proportionnelle: plus il y a d'impacts, plus la pression est élevée, et inversement.
Septième:
Un modèle de gaz parfait est un modèle dans lequel les conditions suivantes doivent être remplies:
- Les molécules de gaz peuvent et sont considérées comme des boules parfaitement élastiques.
- Ces balles peuvent interagir entre elles et avec les murs de n'importe quelnavire dans un seul cas - collision absolument élastique.
- Ces forces qui décrivent la poussée mutuelle entre les atomes et les molécules d'un gaz sont absentes ou peuvent en fait être négligées.
- Les atomes et les molécules sont considérés comme des points matériels, c'est-à-dire que leur volume peut également être négligé.
Huitième:
Donnons toutes les équations de base et montrons les formules dans le sujet "Théorie moléculaire-cinétique":
p=1/3m(0)nv^2 - l'équation de base du modèle de gaz parfait, dérivée par le physicien allemand Rudolf Clausius.
p=2/3nE - l'équation de base de la théorie moléculaire-cinétique d'un gaz parfait. Dérivé de l'énergie cinétique moyenne des molécules.
р=1/3ρv^2 - la même équation, mais considérée à travers la densité et la vitesse quadratique moyenne des molécules de gaz parfaits.
m(0)=M/N(a) - la formule pour trouver la masse d'une molécule à travers le nombre d'Avogadro.
v^2=(v(1)+v(2)+v(3)+…)/N - formule pour trouver la vitesse quadratique moyenne des molécules, où v(1), v(2), v (3) et ainsi de suite - la vitesse de la première molécule, la deuxième, la troisième et ainsi de suite jusqu'à la nième molécule.
n=N/V - formule pour trouver la concentration de molécules, où N est le nombre de molécules dans un volume de gaz à un volume donné V.
E=mv^2/2=3/2kT - formules pour trouver l'énergie cinétique moyenne des molécules, où v^2 est la vitesse quadratique moyenne des molécules, k est une constante valeur nommée d'après la physique autrichienne de Ludwig Boltzmann, et T est la température du gaz.
p=nkT - formule de pression en termes de concentration, constanteBoltzmann et la température absolue T. De là découle une autre formule fondamentale, découverte par le scientifique russe Mendeleev et le physicien-ingénieur français Claiperon:
pV=m/MRT, où R=kN(a) est la constante universelle pour les gaz.
Montrons maintenant les constantes pour différents iso-processus: isobare, isochore, isotherme et adiabatique.
pV/T=const - effectué lorsque la masse et la composition du gaz sont constantes.
рV=const - si la température est également constante.
V/T=const - si la pression du gaz est constante.
p/T=const - si le volume est constant.
C'est peut-être tout ce que vous devez savoir sur ce sujet.
Aujourd'hui, nous avons plongé dans un domaine scientifique tel que la physique théorique, ses multiples sections et blocs. Plus en détail, nous avons abordé un domaine de la physique tel que la physique moléculaire fondamentale et la thermodynamique, à savoir la théorie cinétique moléculaire, qui, semble-t-il, ne présente aucune difficulté dans l'étude initiale, mais présente en fait de nombreux pièges.. Il élargit notre compréhension du modèle des gaz parfaits, que nous avons également étudié en détail. En outre, il convient de noter que nous nous sommes également familiarisés avec les équations de base de la théorie moléculaire dans leurs différentes variantes et avons également examiné toutes les formules les plus nécessaires pour trouver certaines quantités inconnues sur ce sujet, ce qui sera particulièrement utile lors de la préparation de l'écriture. tous les tests, examens et tests, ou pour élargir les perspectives générales et les connaissances de la physique.
Nous espérons que cet article vous a été utile et que vous n'en avez extrait que les informations les plus nécessaires, renforçant vos connaissances dans des piliers de la thermodynamique tels que les dispositions de base de la théorie de la cinétique moléculaire.






