À notre époque, la physique est devenue une science très courante. Il est littéralement présent partout. L'exemple le plus élémentaire: un pommier pousse dans votre jardin et les fruits y mûrissent, le moment vient et les pommes commencent à tomber, mais dans quelle direction tombent-elles? Grâce à la loi de la gravitation universelle, notre fœtus tombe au sol, c'est-à-dire qu'il descend, mais pas vers le haut. C'était l'un des exemples les plus célèbres de la physique, mais attention à la thermodynamique, ou plus précisément aux équilibres de phase, qui ne sont pas moins importants dans notre vie.
Thermodynamique

Tout d'abord, regardons ce terme. ΘερΜοδυναΜική - c'est à quoi ressemble le mot en grec. La première partie ΘερΜo signifie "chaleur", et la seconde δυναΜική signifie "force". La thermodynamique est une branche de la physique qui étudie les propriétés d'un système macroscopique, ainsi que les différentes manières de convertir et de transférer l'énergie. Dans cette section, divers états et processus sont spécialement étudiés afin que la notion de température puisse être introduite dans la description (il s'agit d'une grandeur physique qui caractérise un système thermodynamique et qui se mesure à l'aidecertains appareils). Tous les processus en cours dans les systèmes thermodynamiques ne sont décrits que par des quantités microscopiques (pression et température, ainsi que la concentration des composants).
Équation de Clapeyron-Clausius
Tous les physiciens connaissent cette équation, mais décomposons-la pièce par pièce. Il fait référence aux processus d'équilibre de la transition de certaines matières d'une phase à une autre. Cela se voit clairement dans de tels exemples: fusion, évaporation, sublimation (une des manières de conserver les produits, qui se fait en éliminant complètement l'humidité). La formule montre clairement les processus en cours:
- n=VP/RT;
- où T est la température de la substance;
- P-pression;
- Chaleur de transition de phase spécifique à R;
- V-change dans un volume spécifique.
L'histoire de la création de l'équation

L'équation de Clausius-Clapeyron est une excellente explication mathématique de la deuxième loi de la thermodynamique. Aussi appelée « inégalité de Clausius ». Naturellement, le théorème a été développé par le scientifique lui-même, qui voulait expliquer la relation entre le flux de chaleur dans le système et l'entropie, ainsi que son environnement. Cette équation a été développée par Clausius dans ses tentatives d'expliquer et de quantifier l'entropie. Au sens littéral, le théorème nous donne la possibilité de déterminer si un processus cyclique est réversible ou irréversible. Cette inégalité nous offre une formule quantitative pour comprendre la seconde loi.
Le scientifique a été l'un des premiers à travailler sur l'idée d'entropie, et lui a même donnénom du processus. Ce qui est maintenant connu sous le nom de théorème de Clausius a été publié pour la première fois en 1862 dans le sixième ouvrage de Rudolf, Sur l'utilisation du théorème d'équivalence de transformation pour le travail intérieur. Le scientifique a tenté de montrer une relation proportionnelle entre l'entropie et le flux d'énergie par chauffage (δ Q) dans le système. Dans la construction, cette énergie thermique peut être convertie en travail, et elle peut être transformée en chaleur par un processus cyclique. Rudolph a prouvé que "la somme algébrique de toutes les transformations se produisant dans un processus cyclique ne peut être inférieure à zéro ou, dans les cas extrêmes, égale à zéro."
Système isolé fermé
Le système isolé est l'un des suivants:
- Le système physique est loin des autres qui n'interagissent pas avec eux.
- Le système thermodynamique est fermé par des parois rigides et immobiles à travers lesquelles ni la matière ni l'énergie ne peuvent passer.
Malgré le fait que le sujet est intérieurement lié à sa propre gravité, un système isolé est généralement porté au-delà des limites de la gravitation externe et d'autres forces distantes.
Ceci peut être mis en contraste avec ce qu'on appelle (dans la terminologie plus générale utilisée en thermodynamique) un système fermé entouré de parois sélectives à travers lesquelles l'énergie peut être transférée sous forme de chaleur ou de travail, mais pas de matière. Et avec un système ouvert dans lequel la matière et l'énergie entrent ou sortent, bien qu'il puisse avoir diverses parois impénétrables dansparties de ses frontières.
Un système isolé obéit à la loi de conservation. Le plus souvent en thermodynamique, la matière et l'énergie sont considérées comme des concepts distincts.
Transitions thermodynamiques
Pour comprendre les transitions de phase quantiques, il est utile de les comparer aux transformations classiques (également appelées inversions thermiques). CPT décrit le point culminant des propriétés thermodynamiques d'un système. Il signale la réorganisation des particules. Un exemple typique est la transition de congélation de l'eau, qui décrit une transition en douceur entre un liquide et un solide. Les croissances de phases classiques sont dues à la compétition entre l'énergie du système et l'entropie de ses fluctuations thermiques.
Un système classique n'a pas d'entropie à température nulle et donc aucune transformation de phase ne peut se produire. Leur ordre est déterminé par le premier potentiel thermodynamique dérivé discontinu. Et, bien sûr, il a le premier ordre. Les transformations de phase d'un ferromagnétique à un paramagnétique sont continues et du second ordre. Ces changements constants d'une phase ordonnée à une phase désordonnée sont décrits par un paramètre d'ordre qui est nul. Pour la transformation ferromagnétique ci-dessus, le paramètre d'ordre sera l'aimantation totale du système.
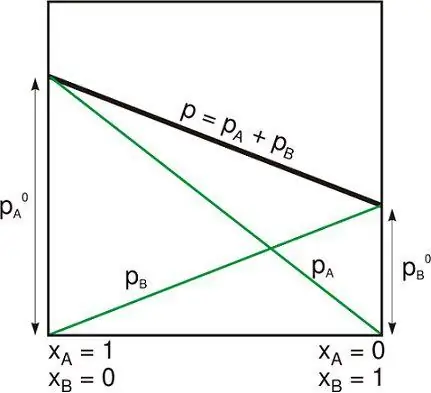
Potentiel de Gibbs
L'énergie libre de Gibbs est la quantité maximale de travail sans expansion qui peut être retirée d'un système fermé thermodynamique (qui peut échanger de la chaleur et travailler avec l'environnement). Telle résultat maximal ne peut être obtenu que dans un processus complètement réversible. Lorsque le système repasse du premier état au second, la réduction de l'énergie libre de Gibbs est égale à celle effectuée par le système dans son environnement, moins le travail des forces de pression.
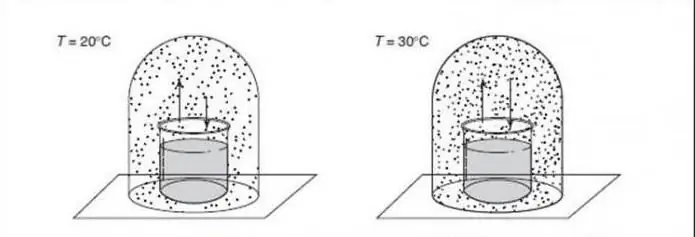
États d'équilibre

L'équilibre thermodynamique et mécanique est un concept axiomatique de la thermodynamique. C'est l'état interne d'un ou plusieurs systèmes reliés par des parois plus ou moins perméables ou imperméables. Dans cet état, il n'y a pas de flux macroscopiques purs de matière ou d'énergie, que ce soit à l'intérieur d'un système ou entre des systèmes.
Dans sa propre conception de l'état d'équilibre interne, aucun changement macroscopique ne se produit. Les systèmes sont simultanément en équilibre thermique, mécanique, chimique (constant), radiatif. Ils peuvent être sous la même forme. Dans ce processus, toutes les vues sont enregistrées en une fois et indéfiniment jusqu'à ce que l'opération physique soit interrompue. En équilibre macroscopique, des échanges équilibrés parfaitement précis ont lieu. La preuve ci-dessus est une explication physique de ce concept.
Bases
Chaque lois, théorèmes, formules ont leurs propres fondements. Regardons les 3 fondements de la loi de l'équilibre de phase.
- La phase est une forme de matière homogène dans sa composition chimique, son état physique et son équilibre mécanique. Les phases typiques sont solides, liquides et gazeuses. Deux liquides non miscibles (ou mélanges de liquides de compositions différentes) séparés par une frontière distincte sont considérés comme deux phases distinctes et des solides non miscibles.
- Le nombre de composants (C) est le nombre de composants chimiquement indépendants du système. Le nombre minimum d'espèces indépendantes requises pour déterminer la composition de toutes les phases du système.
- Le nombre de degrés de liberté (F) dans ce contexte est le nombre de variables intensives indépendantes les unes des autres.
Classement par équilibres de phases
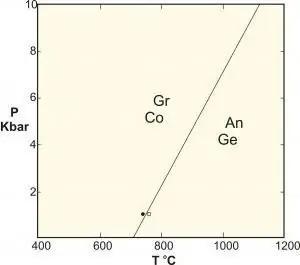
- Les réactions de transfert net continu (souvent appelées réactions à l'état solide) se produisent entre des matières solides de composition différente. Ils peuvent inclure des éléments trouvés dans les liquides (H, C), mais ces éléments sont retenus dans les phases solides, donc aucune phase liquide n'est impliquée en tant que réactifs ou produits (H2O, CO2). Les réactions de transfert pur solide peuvent être continues ou discontinues, ou terminales.
- Les polymorphes sont un type spécial de réaction en phase solide qui comprend des phases de composition identique. Des exemples classiques sont les réactions entre les silicates d'aluminium kyanite-sillimanite-andalousite, la conversion du graphite en diamant à haute pression et l'équilibre du carbonate de calcium.
Lois de l'équilibre

La règle de l'usine de Gibbs a été proposée par Josiah Willard Gibbs dans son célèbre article intitulé "L'équilibre des substances hétérogènes", paru de 1875 à 1878. Il s'applique àsystèmes hétérogènes multicomposants non réactifs en équilibre thermodynamique et est une égalité donnée:
- F=C-P+2;
- où F est le nombre de degrés de liberté;
- C - nombre de composants;
- P - nombre de phases en équilibre thermodynamique entre elles.
Le nombre de degrés de liberté est le nombre de variables intensives inoccupées. Le plus grand nombre de paramètres thermodynamiques, tels que la température ou la pression, qui peuvent varier simultanément et arbitrairement sans s'influencer les uns les autres. Un exemple de système à un composant est celui avec un seul produit chimique pur, tandis que les systèmes à deux composants, tels que des mélanges d'eau et d'éthanol, ont deux composants indépendants. Les transitions de phase typiques (équilibre de phase) sont les solides, les liquides, les gaz.
Règle de phase à pression constante
Pour les applications en science des matériaux traitant des changements de phase entre différentes structures solides, une pression constante se produit souvent (par exemple une atmosphère) et est ignorée en tant que degré de liberté, donc la règle devient: F=C - P + 1.
Cette formule est parfois introduite sous le nom de "règle des phases condensées", mais comme on le sait, elle n'est pas applicable à ces systèmes soumis à de fortes pressions (par exemple en géologie), car les conséquences de ces les pressions peuvent avoir des conséquences catastrophiques.
Il peut sembler que l'équilibre de phase n'est qu'un vain mot, et il y a peu de processus physiques dans lesquels ce momentest impliqué, mais, comme nous l'avons vu, sans cela, de nombreuses lois que nous connaissons ne fonctionnent pas, vous devez donc vous familiariser un peu avec ces règles uniques, colorées, bien qu'un peu ennuyeuses. Cette connaissance a aidé de nombreuses personnes. Ils ont appris à les appliquer à eux-mêmes, par exemple, les électriciens, connaissant les règles de travail avec les phases, peuvent se protéger des dangers inutiles.






